- Диметилртуть
-
Диметилртуть 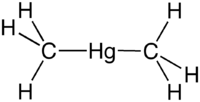
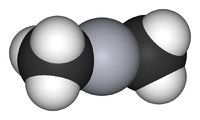
Общие Систематическое наименование Диметилртуть Химическая формула CH3 - Hg - CH3 Физические свойства Молярная масса 230.6612 г/моль Плотность 2.96 г/см³ Термические свойства Температура плавления -43 °C Температура кипения 87-97 °C Температура вспышки 5 °C Классификация Рег. номер CAS 593-74-8 RTECS Ðòóòüîðãàíè÷åñêèå ñîåäèíåíèÿ Диметилртуть — ртутьорганическое соединение с химической формулой Hg(CH3)2. Эта бесцветная жидкость является одним из сильнейших нейротоксинов. Утверждается, что она имеет несколько сладковатый запах; однако, вдыхание паров диметилртути в количестве, достаточном для его восприятия, было бы крайне опасным для жизни.
Содержание
Синтез, структура и реакции
Благодаря своей относительной стабильности, диметилртуть оказалась одним из первых открытых металлоорганических соединений. Она была получена обработкой амальгамы натрия галогенидами метила:
- Hg + 2 Na + 2 CH3I → Hg(CH3)2 + 2 NaI
Также возможно получение алкилированием сулемы метиллитием. Образующаяся молекула приобретает линейную структуру со связями Hg-C длиной 2.083 Å.[1]
Реакции
Наиболее впечатляющей особенностью соединения является отсутствие реакционности с водой, в отличие от аналогичных кадмийорганических и цинкорганических соединений, которые быстро гидролизуются. Эта разница определяется низкой сродностью Hg(II) к лигандам кислорода. Соединение реагирует с хлоридом ртути, образуя смешанное хлоро-метиловое соединение:
- (CH3)2Hg + HgCl2 → 2 CH3HgCl
В то время как диметилртуть — летучая жидкость, CH3HgCl — кристаллическое вещество.
Применение
Из-за рискованности работы с соединением, диметилртуть практически не имеет применений. В токсикологии она используется как эталонный токсин. Также она применяется при калибровке ЯМР спектрографов для детектирования ртути, хотя для этой цели обычно предпочитают гораздо менее токсичные соли ртути.[2][3]
Безопасность
Диметилртуть чрезвычайно опасна. Продемонстрирована смертельность дозы всего в 0.1 мл.[4] Риск ещё более увеличивается в силу высокого давления паров этой жидкости.
Диметилртуть быстро (за считанные секунды) проникает через латекс, ПВХ, полиизобутилен и неопрен, и впитывается через кожу. Таким образом, большинство стандартных лабораторных перчаток не являются надёжной защитой, и единственным способом безопасно обращаться с диметилртутью является использование высокозащищённых ламинированных перчаток под вторыми, доходящими до локтя неопреновыми или иными толстыми защитными перчатками. Отмечается также необходимость ношения длинного лицевого щитка и работы под вытяжным колпаком.[4][5]
Токсичность диметилртути была ещё раз подчёркнута смертью химика-неорганика Карен Веттерхан (англ. Karen Wetterhahn), последовавшей через несколько месяцев после того, как она пролила несколько капель соединения себе на руку, одетую в перчатку из латекса.[4]
Диметилртуть легко преодолевает гематоэнцефалический барьер, вероятно, благодаря образованию комплексного соединения с цистеином. Она очень медленно выводится из организма, и, таким образом, имеет тенденцию к биоаккумуляции. Симптомы отравления могут проявляться месяцы спустя, зачастую чересчур поздно для эффективного лечения.
См. также
Источники
- ↑ Holleman, A. F.; Wiberg, E. «Inorganic Chemistry» Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ↑ Chris Singer 199Hg Standards (10 марта 1998). Архивировано из первоисточника 17 апреля 2012. Проверено 3 мая 2009.
- ↑ Roy Hoffman Mercury NMR (21 февраля 2007). Архивировано из первоисточника 17 апреля 2012. Проверено 3 мая 2009.
- ↑ 1 2 3 Hazard Information Bulletin — Dimethylmercury. OSHA Safety and Health Information Bulletins (SHIBs), 1997—1998
- ↑ Simon Cotton Dimethylmercury and mercury poisoning. The Karen Wetterhahn story.. Архивировано из первоисточника 17 апреля 2012.
Ссылки
- ATSDR — ToxFAQs: Mercury
- ATSDR — Public Health Statement: Mercury
- ATSDR — ALERT! Patterns of Metallic Mercury Exposure, 6/26/97
- ATSDR — MMG: Mercury
- ATSDR — Toxicological Profile: Mercury
- National Pollutant Inventory — Mercury and compounds Fact Sheet
Соединения ртутиАмидохлорид ртути (Hg(NH2)Cl) • Ацетат ртути(I) (Hg2(CH3COO)2) • Бромид ртути(I) (Hg2Br2) • Бромид ртути(II) (HgBr2) • Гидрид ртути(II) (HgH2) • Диметилртуть (Hg(CH3)2) • Диэтилртуть (Hg(C2H5)2) • Иодид ртути(I) (Hg2I2) • Иодид ртути(II) (HgI2) • Карбонат ртути(I) (Hg2(CO3)2) • Нитрат ртути(I) (Hg2(NO3)2) • Нитрат ртути(II) (Hg(NO3)2) • Оксид ртути(I) (Hg2O) • Оксид ртути(II) (HgO) • Пероксид ртути (HgO2) • Селенид ртути (HgSe) • Сульфат ртути(I) (Hg2SO4) • Сульфат ртути(II) (HgSO4) • Сульфид ртути(I) (Hg2S) • Сульфид ртути(II) (HgS) • Теллурид ртути (HgTe) • Тетраиодомеркурат(II) калия (K2[HgI4]) • Тиоцианат ртути(I) (Hg2(CNS)2) • Тиоцианат ртути(II) (Hg(CNS)2) • Фторид ртути(I) (Hg2F2) • Фторид ртути(II) (HgF2) • Фульминат ртути(II) (Hg(CNO)2) • Хлорид ртути(I) (Hg2Cl2) • Хлорид ртути(II) (HgCl2) • Хлорид этилртути (С2H5HgCl) • Цианид ртути(II) (Hg(CN)2) •
Чрезвычайно опасные вещества
Акролеин • Бензапирен • Бериллий • Винилхлорид • Диметилртуть • Диоксины • Диэтилртуть • Зоман • Линдан • Озон • Оксид свинца • Пентахлордифенил • Полоний • Плутоний • Протактиний • Ртуть (суммарно) • Стрихнин • Таллий • Теллур • Тетраэтилолово • Тетраэтилсвинец • Трихлордифенил • Фтороводород • Хлорокись фосфора • Цианид калия • Цианид натрия • Циановодород • Этилмеркурхлорид
Категории:- Соединения ртути
- Чрезвычайно опасные вещества
- Нейротоксины
- Металлоорганические соединения
Wikimedia Foundation. 2010.
