- Хлораты
-
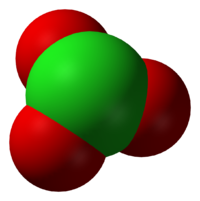
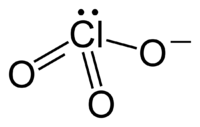
Хлора́ты — группа химических соединений, соли хлорноватой кислоты HClO3. Хлорат анион имеет структуру тригональной пирамиды (dCl—О = 0,1452-0,1507 нм, угол OClO = 106°). Анион ClO3− не образует ковалентных связей через атом О и не склонен образовывать координационные связи.
Свойства
Обычно кристаллические вещества, растворимые в воде и некоторых полярных органических растворителях. В твердом состоянии при комнатной температуре довольно стабильны. При нагреве или в присутствии катализатора разлагаются с выделением кислорода. С горючими веществами могут образовывать взрывчатые смеси.
Хлораты являются сильными окислителями как в растворе, так и в твердом состоянии: смеси безводных хлоратов с серой, углем и другими восстановителями, взрываются при быстром нагревании и ударе. Хотя хлор в хлоратах находится не в высшей степени окисления, доокислить его в водном растворе удается только электрохимически или под действием XeF2.
Хлораты большинства металлов получены в виде гидратов, в безводном состоянии выделены хлораты щелочных и щелочно-земельных металлов, Ag, Tl(II), Pb(II), а также NH4Cl3, N(CH3)4ClO3. Хлораты металлов переменной валентности обычно неустойчивы и склонны к взрывному распаду. Все хлораты щелочных металлов разлагаются с выделением большого количества тепла на MCl и О2, с промежуточным образованием перхлоратов.
Получение
- Хлорирование гидроксидов металлов
-
- 3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
- Обменные реакции хлоратов с другими солями
- Электрохимическое окисление хлоридов металлов в водных растворах
Применение
- В составе взрывчатых веществ
- В зажигательных смесях
- Для химического травления металлов
- Для получения кислорода в лабораторных масштабах
- Как десиканты для предуборочного высушивания растений
 Категория:
Категория:- Хлораты
Wikimedia Foundation. 2010.